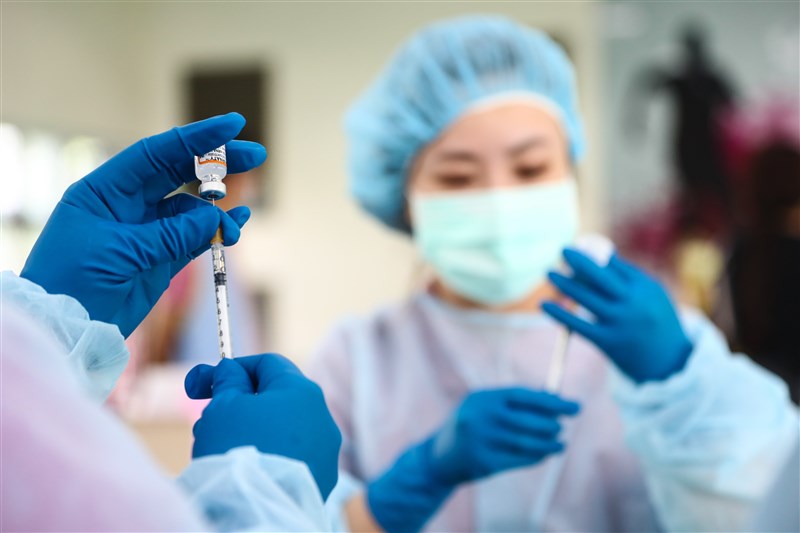
 雙價疫苗(次世代疫苗)分2種,現在進行採購及審查EUA的是原始株加BA.1,目前原始株加BA.5的次世代疫苗只有美國獲得通過。圖/中央社
雙價疫苗(次世代疫苗)分2種,現在進行採購及審查EUA的是原始株加BA.1,目前原始株加BA.5的次世代疫苗只有美國獲得通過。圖/中央社
【本報台北訊】國內BA.5疫情升溫,為防範Omicorn新變異株,針對莫德納次世代疫苗緊急使用授權(EUA)審查會議今下午3時舉行,指揮中心指揮官王必勝表示,在通過的前提下,下周一召開ACIP會議,決定如何施打、施打族群、間隔時間等,再決定進貨量,疫苗採購小組已準備好,完成後就會聯絡運送的時間。
王必勝表示,開ACIP會議的原因,會將依據疫苗公司提供的臨床試驗,以及評估現行施打程度,再決定接種族群及施打間隔時間,這都需要等9月5日下周一會議後才會知道。
至於會不會開放所有人接種次世代疫苗?王必勝表示,有可能,但有年齡限制,從哪階段年齡開始,還需開會討論。莫德納次世代疫苗預計是9月底進貨,約在9月底、10月初開放施打。
雙價疫苗(次世代疫苗)分2種,一種是原始株加BA.1,另一種是原始株加BA.5,現在進行採購及審查EUA的是原始株加BA.1,目前原始株加BA.5的次世代疫苗只有美國獲得通過。
經深入研究,這次美國審查為非典型審查,屬於非常規審查,是由動物實驗及人體試驗資料同時審查,因此國內現階段仍採取歐盟及世界衛生組織(WHO)的建議,購買原始株加BA.1的雙價疫苗。
王必勝指出,據了解,目前原始株加BA.1的雙價疫苗,也可以防護BA.4、BA.5,但這要通過EUA才有明確的答案。
另對於原始株加BA.5的雙價疫苗仍會持續關心,等待有更多的人體施打安全性、效價等資料,並送到食藥署進行審查,才會進一步討論,因尚未收到此疫苗的任何資料,目前就是依原定計畫。
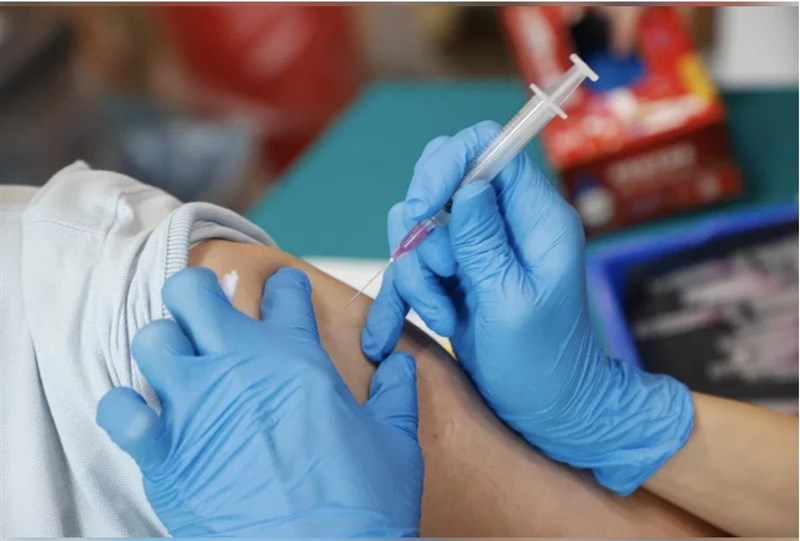 原始株加BA.5的雙價疫苗,等待有更多的人體施打安全性、效價等資料,並送到食藥署進行審查,才會進一步討論圖。圖/資料照片
原始株加BA.5的雙價疫苗,等待有更多的人體施打安全性、效價等資料,並送到食藥署進行審查,才會進一步討論圖。圖/資料照片