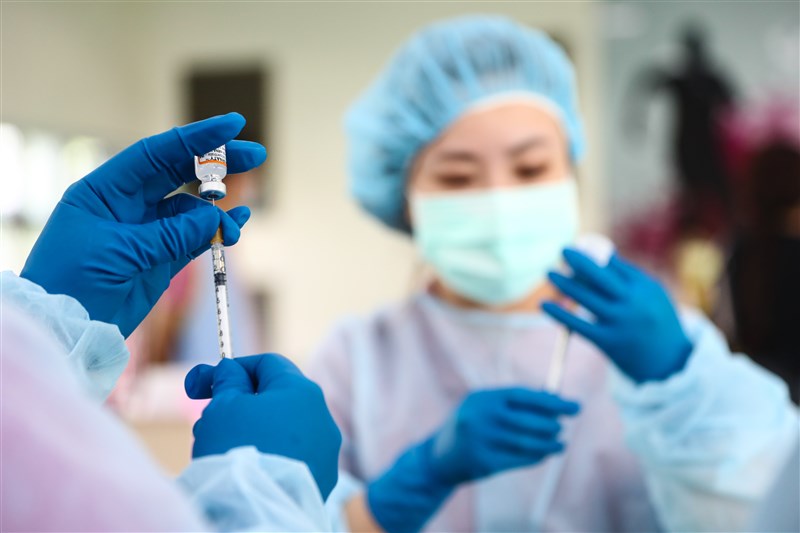
 次世代疫苗EUA通過後,會安排衛福部傳染病防治諮詢會預防接種組(ACIP)開會,同時向廠商下訂疫苗,若順利10月可到貨。圖/中央社
次世代疫苗EUA通過後,會安排衛福部傳染病防治諮詢會預防接種組(ACIP)開會,同時向廠商下訂疫苗,若順利10月可到貨。圖/中央社
【本報台北訊】國內Omicron BA.5疫情升溫,但次世代疫苗仍在審查中,日前要求莫德納次世代疫苗緊急使用授權(EUA)審查,限期廠商於8月26日前補件資料,但指揮中心指揮官王必勝表示,尚未收到廠商補件,力拚下周完成審查。
食藥署8月23日針對莫德納次世代疫苗召開審查會議,王必勝在24日記者會表示,經過整理資料後,食藥署認定莫德納次世代疫苗需補件,並限期8月26日前提交,將盡快安排8月29日審查。
王必勝也透露,BNT次世代疫苗在上周收到少部分文件,也正請食藥署進行相關審查,但資料有限,要等完整文件送交才會進行EUA審查。
次世代疫苗採用同步審查,不管資料多少,都希望廠商同步繳交,審查進度才不會延宕。
後續EUA通過後,會安排衛福部傳染病防治諮詢會預防接種組(ACIP)開會,同時向廠商下訂疫苗,若順利10月可到貨。